抗生素在兽医学中经常被用作生长促进剂和疾病的治疗和预防。无正当理由使用抗生素可能导致动物源性食品(包括肉类和牛奶)中的残留超标——对人类健康构成潜在风险。
食物中的抗生素残留物会引发毒性和一系列副作用,包括过敏反应、恶心和皮疹。在食品中长期食用低剂量的抗生素会导致耐药细菌的传播。
因此,世界上每个国家都调节在动物中使用抗生素。
加拿大和欧盟在食物中设定了最大的残留水平(MRLS)的药物残留物,而美国指的是耐受性水平。
牛奶中使用的抗生素残留类别吸引了监管部门的注意,包括磺胺类、氟喹诺酮类、β-内酰胺类、大环内酯类和四环素类。表1提供了本研究分析的各类抗生素在牛奶中的耐受限度。
表格1。牛奶中不同种类抗生素及其耐药限度一览表。资料来源:PerkinElmer食品安全和质量公司
| 化合物 |
抗生素类 |
公差等级一个 |
| 磺胺甲嘧啶 |
磺酰胺 |
10 ng / mlb |
| 磺胺甲恶唑 |
磺酰胺 |
10 ng / mlb |
| Sulfadimethoxinef |
磺酰胺 |
10 ng / mlb |
| Tilmicosin |
大环内酯物 |
100毫微克/毫升c |
| 泰乐菌素 |
大环内酯物 |
50 ng / ml |
| 红霉素 |
大环内酯物 |
50 ng / ml |
| 青霉素 |
β内酰胺 |
5 ng / ml |
| 邻氯青霉素 |
β内酰胺 |
10 ng / ml |
| 氧氟沙星 |
氟喹诺酮类 |
5 ng / mld |
| 环丙沙星 |
氟喹诺酮类 |
5 ng / mld |
| Sarafloxacin |
氟喹诺酮类 |
5 ng / mld |
| 四环素 |
四环素 |
300毫微克/毫升e |
| Chlortetracycline. |
四环素 |
300毫微克/毫升e |
一个来自9/27/05 FDA / CFSAN牛奶安全分支备忘录的牛奶耐受性或安全水平1
b列出的数量是“安全水平”,而不是一个公差
c对牛奶没有设定耐受量;方法目标水平设为100 ng/ml(肌肉耐受)
d没有确定容忍或安全水平;方法以5 ng/ml为目标水平
e容忍包括总和和单独的残留物;方法目标级别设置为100 ng / ml
f禁止在哺乳奶牛中使用磺酰胺类药物(磺胺二甲氧嘧啶除外)1
本文提出了一种快速、灵敏的方法LC / MS / MS法这是对牛奶中多级抗生素的定量和确认分析的理想选择。本研究分析的抗生素包括:
-
环丙沙星
-
Sarafloxacin
-
氧氟沙星
-
青霉素
-
邻氯青霉素
-
Tilmicosin
-
泰乐菌素
-
红霉素
-
磺胺甲嘧啶
-
磺胺甲恶唑
-
Sulfadimethoxine
-
四环素
-
金霉素。
本方法采用两个内标环丙沙星d8和flunixin-d3..一种改进的、基本的QuEChERS方法被用于从牛奶中提取一系列抗生素。
该方法具有良好的灵敏度、回收率、线性度、精密度和选择性,适用于众多监管机构规定的低耐受水平的牛奶中抗生素的分析。
硬件和软件
样品及样品制备
一个PerkinElmer阿尔特斯™UPLC®系统用于色谱分离。该仪器包括Altus A-30溶剂/样品模块,柱加热器和一体化真空脱气器。
QSight™210 Triple Quadrupole MS/MS检测器用于检测,而仪器控制、分析和数据处理均通过Simplicity 3Q™软件平台完成。
方法参数
表2提供了LC方法和MS源参数的完整列表。
表2。LC方法和MS源参数。资料来源:PerkinElmer食品安全和质量公司
| 信用证条件 |
| 专栏: |
PerkinElmer Brownlee™SPP C18, 2.7 μm, 2.1 x 100 mm (Part # N9308404) |
| 流动相: |
溶剂:5mM甲酸铵,0.1%甲酸水溶液
溶剂B:95%乙腈(ACN)/ 5%甲醇与0.1%甲酸
|
时间(分钟) |
%的 |
% B |
曲线 |
| 1 |
最初的 |
95.0 |
5.0 |
| 2 |
0.50 |
95.0 |
5.0 |
6 |
| 3. |
7.50 |
40.0 |
60.0 |
6 |
| 4 |
10.00 |
0.0 |
100.0 |
6 |
| 5 |
15.00 |
0.0 |
100.0 |
6 |
| 6 |
15.30 |
95 |
5.0 |
6 |
|
| 分析时间: |
12分钟;柱洗时间为100% B: 3分钟;再平衡时间:4.2分钟 |
| 流量: |
0.4毫升/分钟 |
| 压力: |
4200 psi/285 bar(最大) |
| 烤箱温度: |
30ºC |
| 注入体积: |
10μL |
| 样品温度: |
7ºC |
| 女士的条件 |
| 电离模式: |
ESI - 阳性 |
| 干燥气体(氮气)设置: |
75个任意单位 |
| HSID™临时: |
320°C |
| 电喷雾电压: |
5500 V |
| 源温度: |
425ºC |
| 雾化器气体(氮气)设置): |
175个任意单位 |
| 检测模式: |
MRM模式 |
溶剂,标准和样品制备
本研究使用的溶剂、试剂和稀释剂均为LC/MS级,所有抗生素标准均由Sigma-Aldrich提供®为了防止其降解,将其储存在4°C的冰箱中。
在甲醇中制备了用于校准和加药的库存和混合药物溶液。除了以水为溶剂的β-内酰胺外,所有抗生素都是如此。虽然其他抗生素标准品可以存放在玻璃或塑料容器中,但有必要将β-内酰胺标准品储存在塑料瓶中。
从Supelco获得吸附剂端盖C18,在自动进样器托盘中保持在7℃的小瓶以防止分析物降解。所有库存和工作标准都储存在制冷下,直至需要,仅使用琥珀色2mL LC小瓶。这也是为了防止退化。
采用环丙沙星d两种内标进行校准和定量8磺胺类,氟喹诺酮类,四环素类和氟尼辛d3.大环内酯类和β-内酰胺类。
来自当地市场的有机全脂牛奶样品被用作受控的空白基质。同时对五种不同类型的牛奶样品进行不同脂肪含量的分析,以研究抗生素的存在。采用基本的、改进的QuEChERS方法制备样品。2,3
-
将20 ml有机溶剂(甲醇或乙腈)添加到5 ml空白有机牛奶或添加了不同水平抗生素和15 ng/ ml内标强化的牛奶中。
-
在以7800rpm离心10分钟之前,样品在脉冲涡旋1分钟内进行1分钟。
-
除去上清液,加入1.2g C18以进行分散体脂肪去除。
-
样品在7800 rpm离心5分钟前进行脉冲涡旋。
-
取出12.5 ml上清液,用干氮将其干燥至1.5 ~ 2ml。在40°C下进行约1小时。
-
样品在水中用15%的甲醇重建,使提取液的总体积达到2.5 ml。
-
提取液经PVDF滤膜过滤(0.22µm)。
对于基质匹配校准,在步骤7之后加入加标和内标溶液,以提供从0.1 ng/ml到1000 ng/ml的样品中等效的分析物浓度。在每个校准水平上有5个重复。
MS / MS参数
所有残留的分析均采用电喷雾正电离模式。优化了源参数(如源温度、气体流量和位置设置)。
这是通过将0.5μg/ ml的磺胺甲磺胺溶液在10μl/ min注入到90:10水的流中来完成的:乙腈,甲酸0.1%甲酸和5mM甲酸甲酸盐,流速为0.5ml / min。
将每个残留物的溶液注入0.5μg/ ml以确定每个MRM转变的最佳碰撞能量。四极峰宽度(Q1和Q3)设定为0.7 Amu。
表3提供了每个MRM转换的参数,每个抗生素残留监测这些MRM转换中的三个,以限制该方法中假阳性和阴性的数量。4
结果和讨论
表4总结了各抗生素校准曲线的LOQ和回归值每一种分析的抗生素的定量限被发现比牛奶中可接受的耐受水平低5到100倍。
表3。LC/MS/MS方法的MS/MS参数。资料来源:PerkinElmer食品安全和质量公司
| 被分析物 |
保留时间 |
保压时间 |
前体离子 |
定量离子 |
CE |
定性离子1 |
CE |
定性离子2 |
CE |
| 磺胺甲嘧啶 |
3.37分钟 |
10毫秒 |
279.1 |
186 |
20 V |
156 |
25 V |
107.9 |
40 V |
| Sulfamthoxazole |
4.38分钟 |
10毫秒 |
254.1 |
107.9 |
40 V |
91.7 |
55 V |
156 |
30 V |
| Sulfadimethoxine |
5.15分钟 |
10毫秒 |
311.1 |
156 |
25 V |
91.7 |
40 V |
107.9 |
50 V |
| Tilmicosin |
4.93分钟 |
30岁的女士 |
435.3 |
695.4 |
20 V |
174 |
30 V |
87.9 |
55 V |
| 泰乐菌素 |
5.70分钟 |
30岁的女士 |
916.5 |
174 |
46 V. |
100.9 |
64 V |
144.9 |
48 V |
| 红霉素 |
5.41分钟 |
20女士 |
734.4 |
158 |
40 V |
576.2 |
22 V |
115.9 |
66 V |
| 青霉素 |
5.38分钟 |
30岁的女士 |
334.9 |
160 |
22 V |
176 |
22 V |
113.9 |
48 V |
| 邻氯青霉素 |
6.6分钟 |
30岁的女士 |
436.2 |
277.1 |
18 V |
113.9 |
62 V |
178 |
50 V |
| 氧氟沙星 |
3.30分钟 |
10毫秒 |
361.9 |
317.9 |
25 V |
343.9 |
25 V |
260.9 |
35 V. |
| 环丙沙星 |
3.38分钟 |
10毫秒 |
331.9 |
313.9 |
24 V. |
230.9 |
51 V |
187.9 |
75 V |
| Sarafloxacin |
3.93分钟 |
10毫秒 |
385.9 |
367.9 |
28 V |
341.9 |
24 V. |
298.9 |
36 V. |
| 四环素 |
3.52分钟 |
30岁的女士 |
445.1 |
410.1 |
16 V |
154 |
24 V. |
97.9 |
36 V. |
| Chlortetracycline. |
4.33分钟 |
30岁的女士 |
479. |
444. |
26 V |
462. |
22 V |
154 |
36 V. |
| Ciprofloxacin-d8 |
3.36分钟 |
10毫秒 |
340.1 |
235. |
48 V |
- |
- |
- |
- |
| Flunixin-D.3. |
7.20分钟 |
10毫秒 |
300 |
282 |
30 V |
- |
- |
- |
- |
表4。乳提取物中不同抗生素残留的定量限及线性相关系数。资料来源:PerkinElmer食品安全和质量公司
| 化合物 |
牛奶中定量限 |
线性校准曲线浓度范围 |
相关系数R2 |
| 磺胺甲嘧啶 |
0.1 ng / ml |
0.1-1000 ng / ml |
0.9986 |
| 磺胺甲恶唑 |
0.1 ng / ml |
0.1-1000 ng / ml |
0.9996. |
| Sulfadimethoxine |
0.1 ng / ml |
0.1-1000 ng / ml |
0.9991. |
| Tilmicosin |
0.1 ng / ml |
0.1-1000 ng / ml |
0.9990 |
| 泰乐菌素 |
1 ng / ml |
1 - 1000 ng / ml |
0.9980 |
| 红霉素 |
0.3 ng / ml |
0.3 -1000 ng / ml |
0.9958 |
| 青霉素 |
1 ng / ml |
1 - 1000 ng / ml |
0.9981 |
| 邻氯青霉素 |
1 ng / ml |
1 - 1000 ng / ml |
0.9985 |
| 氧氟沙星 |
0.1 ng / ml |
0.1-1000 ng / ml |
0.9982 |
| 环丙沙星 |
0.1 ng / ml |
0.1-1000 ng / ml |
0.9978 |
| Sarafloxacin |
0.1 ng / ml |
0.1-1000 ng / ml |
0.9968 |
| 四环素 |
0.3 ng / ml |
0.3 -1000 ng / ml |
0.9956 |
| Chlortetracycline. |
0.3 ng / ml |
0.3 -1000 ng / ml |
0.9984 |
这证实了该方法对低耐受水平的牛奶中的抗生素具有足够的敏感性。
图1显示了单一抗生素-磺胺甲嗪的三个MRM转换。这些在牛奶基质中以5 ng/ml的水平添加,表明对噪声有良好的信号。在24小时内,每个分析物的保留时间可在±0.1分钟内重现。
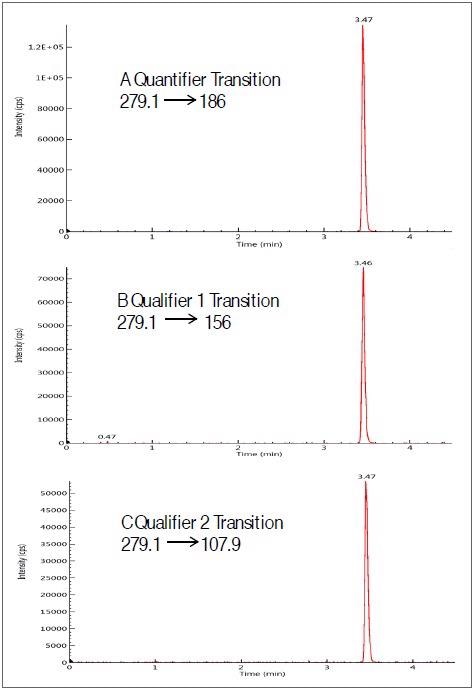
图1所示。磺胺甲嗪在牛奶提取物中以5ng/ml添加量的三个MRM跃进(一个量词- a和两个限定词- b,C)的色谱图。图片来源:PerkinElmer食品安全和质量公司
在空白牛奶样品中添加不同浓度的抗生素(0.1-1000 ng/mL),生成基质匹配的校准曲线。这是在九种不同浓度和内部标准下进行的。
图2提供了磺胺甲嘧啶的示例校准曲线,示出了四个数量级。
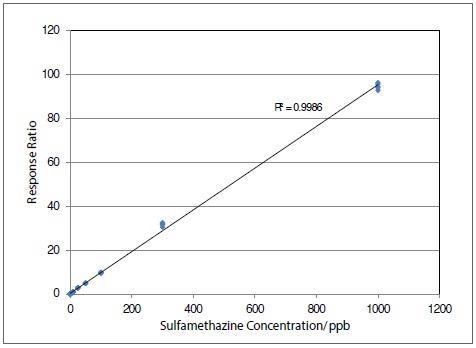
图2。n=5时,磺胺甲嗪在浓度范围从0.1到1000 ng/ml范围内的牛奶提取物的校准曲线。图片来源:PerkinElmer食品安全和质量公司
确定校准曲线是线性的,r的校准适合2大于0.9958的所有分析物。表5显示了每种分析物在不同浓度下5次重复响应的异常精度。
表5。牛奶提取物中不同水平的抗生素残留反应的重复性。资料来源:PerkinElmer食品安全和质量公司
| 化合物 |
2.5 ng / ml相对标准偏差
(n = 5) |
5 ng / ml相对标准偏差
(n = 5) |
10 ng / ml相对标准偏差
(n = 5) |
25 ng / ml相对标准偏差
(n = 5) |
50 ng / ml相对标准偏差
(n = 5) |
100 ng / ml相对标准偏差
(n = 5) |
| 磺胺甲嘧啶 |
2.4% |
2.4% |
1.1% |
1.4% |
0.8% |
0.7% |
| 磺胺甲恶唑 |
3.5% |
4.7% |
2.8% |
1.7% |
2.9% |
1.4% |
| Sulfadimethoxine |
3.0% |
0.8% |
2.0% |
1.6% |
1.2% |
1.7% |
| Tilmicosin |
0.7% |
1.5% |
1.8% |
0.7% |
0.8% |
1.1% |
| 泰乐菌素 |
7.8% |
4.3% |
3.9% |
2.1% |
2.2% |
1.4% |
| 红霉素 |
4.7% |
3.8% |
4.0% |
1.7% |
2.3% |
0.8% |
| 青霉素 |
3.0% |
4.4% |
4.2% |
1.4% |
2.6% |
1.5% |
| 邻氯青霉素 |
4.5% |
4.4% |
3.7% |
2.5% |
1.8% |
1.4% |
| 氧氟沙星 |
2.9% |
1.9% |
2.6% |
1.5% |
1.7% |
1.8% |
| 环丙沙星 |
2.2% |
2.3% |
0.9% |
3.1% |
1.0% |
1.1% |
| Sarafloxacin |
2.4% |
2.8% |
2.0% |
1.5% |
2.0% |
0.7% |
| 四环素 |
6.1% |
5.9% |
6.1% |
4.7% |
2.8% |
1.3% |
| Chlortetracycline. |
5.6% |
5.0% |
5.7% |
3.6% |
4.1% |
2.1% |
数据突出表明,在牛奶提取物中存在的每种分析物的浓度为耐受水平的一半或更高时,响应的RSD小于5%。
表6提供了牛奶中所有13种抗生素在接近其耐受极限浓度水平时的恢复情况。大环内酯类、磺胺类和β-内酰胺类抗生素的绝对回收率在70% ~ 120%之间,重复样品RSD% <20% (n=5)。
氟喹诺酮类的绝对加样回收率在60% ~ 70%之间,而四环素类的绝对加样回收率在30%以下。内标环丙沙星d的回收8和flunixin-d3.- 分别为70%和90%。
由于氟喹诺酮类和氘化氟喹诺酮类在提取过程中可能遭受类似的损失,使用内标来补偿氟喹诺酮类较低的绝对回收率是可以接受的。
氟喹诺酮类和四环素类药物的回收率(表1)已通过使用内标环丙沙星-d提取过程中的损失进行修正8.
氟喹诺酮类药物的回收率在80% - 110%之间,使用氘氟喹诺酮作为内标进行校正,而四环素类药物的回收率约为30%。在今后的实验中,氘四环素可用于补偿四环素的损失。
表6列出了在蛋白质沉淀过程中使用一系列有机溶剂的影响,强调了这些可能如何影响分析物的回收和基质中的离子抑制。
表6。对提取过程中不同溶剂(乙腈和甲醇)对不同抗生素的回收率和基质效应进行了平均和RSD测定。资料来源:PerkinElmer食品安全和质量公司
| 化合物 |
强化级别(ng / ml) |
复苏与甲醇 |
甲醇回收率RSD N=5 |
与甲醇的基质效果 |
复苏与乙腈 |
乙腈加样回收率N=5 |
乙腈的基质效应 |
| 磺胺甲嘧啶 |
10. |
102% |
8% |
110% |
101% |
9% |
102% |
| 磺胺甲恶唑 |
10. |
103% |
10% |
93% |
105% |
13% |
97% |
| Sulfadimethoxine |
10. |
96% |
7% |
111% |
104% |
7% |
106% |
| Tilmicosin |
50 |
89% |
10% |
127% |
82% |
15% |
103% |
| 泰乐菌素 |
50 |
97% |
14% |
83% |
92% |
17% |
97% |
| 红霉素 |
50 |
98% |
11% |
80% |
27% |
17% |
91% |
| 青霉素 |
10. |
103% |
10% |
94% |
84% |
10% |
96% |
| 邻氯青霉素 |
10. |
94% |
13% |
97% |
96% |
13% |
102% |
| 氧氟沙星 |
10. |
101% |
17% |
163% |
97% |
1.7% |
181% |
| 环丙沙星 |
10. |
102% |
16% |
174% |
87% |
1.0% |
163% |
| Sarafloxacin |
10. |
104% |
11% |
162% |
96% |
9% |
142% |
| 四环素 |
50 |
32% |
5% |
152% |
24% |
5% |
120% |
| Chlortetracycline. |
50 |
25% |
8% |
177% |
21% |
10% |
130% |
值得注意的是,除红霉素外,所有分析物的回收率在两种溶剂中相似——红霉素用乙腈和甲醇的回收率分别约为27%和98%。
通过施加乳基质中分析物在乳基质中的响应与溶剂标准的比率来计算基质抑制和增强。当使用样品制备时用于甲醇或乙腈,用于磺酰胺,大溴化甲酰胺和β-内酰胺的基质抑制和增强可忽略不计。
氟喹诺酮类和四环素类都表现出一定程度的离子增强。平均而言,使用甲醇而不是乙腈会产生更高的离子增强效果。它与氟喹诺酮类和四环素类的基质相连。
5个不同脂肪含量(1%至5%)的牛奶样品采用内部标准进行强化。然后使用这里概述的方法对这些样本进行抗生素筛选。
保留时间和定量离子响应确认没有检测到目标抗生素分析物,即使在比方法的定量限(0.1到1 ng/ml)低三倍的水平。
确定牛奶样品的回收率从具有不同脂肪含量的牛奶样品的回收率低于15%,表明,当使用此处概述的样品制备方法时,牛奶的脂肪含量不会影响这些分析物的恢复。
监测三种离子转换而不是两个过渡,以确保准确识别和确认。该方法提供了两种产物离子比而不是一个产品离子比,确保较高的选择性和改善的识别特异性。
通过计算低强度离子的峰面积和高强度离子的峰面积来确定离子比,生成的离子比小于100%。
表7显示了目标分析物的平均离子比。这些在牛奶提取物中显示的浓度水平是耐受水平的一半到10倍。
表7所示。牛奶提取物中不同浓度抗生素残留的2个离子比值及其范围的平均值。资料来源:PerkinElmer食品安全和质量公司
| 化合物 |
离子比1 |
相对离子比1差 |
离子比2 |
相对离子比2差 |
| 磺胺甲嘧啶 |
57% |
±5% |
43% |
±6% |
| 磺胺甲恶唑 |
99% |
±5% |
90% |
±6% |
| Sulfadimethoxine |
38% |
±6% |
29% |
±5% |
| Tilmicosin |
76% |
±5% |
64% |
±5% |
| 泰乐菌素 |
44% |
±6% |
26% |
±11% |
| 红霉素 |
46% |
±5% |
24% |
±6% |
| 青霉素 |
78% |
±5% |
50% |
±10% |
| 邻氯青霉素 |
43% |
±5% |
38% |
±6% |
| 氧氟沙星 |
69% |
±9% |
62% |
±7% |
| 环丙沙星 |
43% |
±5% |
2.5% |
±12% |
| Sarafloxacin |
13% |
±7% |
8.1% |
±7% |
| 四环素 |
23% |
±6% |
21% |
±10% |
| Chlortetracycline. |
68% |
±6% |
37% |
±6% |
发现各种浓度水平的相对离子比例在平均离子比的±11%范围内 - 低于Sanco在食品中化学残留物分析的±30%的可接受的相对耐受水平限制。5
通过注射添加了10 ng/ml氟喹诺酮类、磺胺类、β-内酰胺类和50 ng/ml大环内酯类和四环素类的乳提取物,在6天内评估了该系统的长期稳定性。
关于内标在图3中突出了10ng / ml磺胺甲嘧啶的长期归一化反应在图3中突出显示。
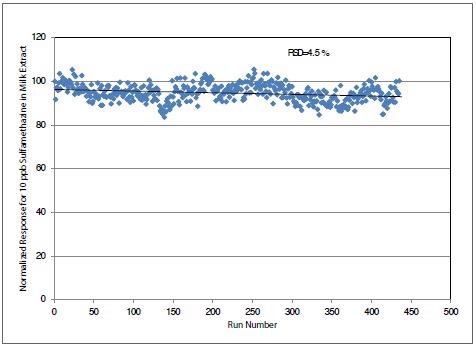
图3。6天内磺胺甲嗪注射剂量为10ng /ml牛奶的长期稳定性数据。图片来源:PerkinElmer食品安全和质量公司
值得注意的是,磺胺甲嗪的反应没有下降,即使在注射6天后。这证明了三联四联质谱系统的良好稳定性。
在13种抗生素残留中,有10种在注射6天后没有降解,而其中3种(红霉素、泰乐星和氧氟沙星)的反应在6天后下降了30%。这可以通过这些抗生素随时间的分解来解释。
结论
本研究有效地证明了该方法的快速、稳健和可靠LC / MS / MS法这对于牛奶中多种抗生素的分析具有足够的选择性和敏感性。
本研究使用了一种改进的QuEChERS样品制备方法,该方法简单,对大多数被调查的抗生素类具有良好的回收率。
该方法促进了牛奶中低PPB范围(0.1至1ppb)的靶化合物的鉴定和定量,同时展示了良好的保留时间稳定性和精度。
长期稳定性数据证实,LC/MS/MS系统能够在不停机维护的情况下分析含脏基质的样品。
参考文献
-
美国FDA/CFSAN牛奶中动物药物残留的耐受和/或安全水平;2005年9月27日的备忘录。
-
S. B. Clark, J. M. Storey, S. B. Turnipseed, FDA实验室信息公告,Lib # 4443,http://www.fda.gov/downloads/亚博老虎机网登录ScienceResearch/FieldScience/UCM239311.pdf。
-
L. Geis-Asteggiante, S. J. Lehotay, A. R.Lightfield, T. Dutko, C. Ng, L. blhm, J. Chrom。A, 2012, 1258, 43。
-
T. Yamaguchi, M. Okihashi, K. Harada, K. Uchida, Y. Konishi, K. Kajimura, K. Hirata, Y. Yamamato, J. Agri。食品化学。, 2015, 63,5133。
-
欧盟委员会关于食品和饲料残留分析分析质量控制和验证程序的指导文件,Sanco12571(2013),/ docs / qualcontrol_en.pdf http://ec.europa.eu/food/plant/pesticides/guidance_文件
致谢
由PerkinElmer公司亚博网站下载的Avinash Dalmia原创的材料制作。

此信息已采购,从PerkinElmer食品安全和质量提供的材料进行审核和调整。亚博网站下载
有关此来源的更多信息,请访问PerkinElmer食品安全和质量。