本文研究了利用拉曼成像对现有药品进行逆向工程。有一些监管途径与FDA,通过公司可以寻求批准仿制药。缩写新药应用(ANDA)路线是最值得注意的。这是指仿制药公司开发了一份完全相同的创新产品副本,而来自创新产品的安全性和有效性数据可以用于其提交的目的。参议员奥林·哈奇(Orrin Hatch)和众议员亨利·韦克斯曼(Henry Waxman)在20世纪80年代通过《药品价格竞争和专利期限恢复法案》(Drug Price Competition and Patent Term Restoration Act)为这一路线提供了支持,因此,它被非正式地称为《哈奇-韦克斯曼法案》(Hatch-Waxman Act)。
当时,美国政府对批准的仿制药数量较少感到担忧。在《哈奇-韦克斯曼法案》之前,创新公司很容易制造法律障碍,阻止其他公司开发仿制药。这使得仿制药的开发成为一个非常没有吸引力的行业。许多这些障碍被《哈奇-韦克斯曼法案》(Hatch-Waxman Act)所消除,该法案随后成功地激励非专利药公司生产负担得起的非专利药。与此同时,它还通过在药物首次发布后给予创新公司足够的专有权期来保护它们,这保持了创新的有利地位。
仿制药批准的替代途径是505(b)(2)。它用于药品申报,其中可能包含从选定参考产品的先前研究中获得的安全性和有效性调查报告。然而,该药物的剂型故意不同于对照品。将现有药物用于新的适应症或将现有药物用于不同的给药途径是505(b)(2)种候选药物的两个主要例子。
由上市参考产品产生的原料药毒性和安全性数据可供制药商在这种情况下使用。然而,其制剂在临床中的疗效和有效性仍需明确证明。
当涉及到anda时,人们对生物豁免领域的兴趣越来越大。这些是调节途径在体外单独的检测可以用来证明仿制药与参比产品相等,从而不需要进行生物等效性研究。一种药物必须表现出Q1, Q2和Q3的同一性,才能考虑获得生物豁免。
表1。
| 第一季度 |
定性相似:被测产品和参比产品含有相同的活性和非活性成分。 |
| 第二季 |
成分数量相似:活性成分和非活性成分数量相同。 |
| 第三季 |
结构相同(目前仅用于局部药物):相同的微观结构 |
https://www.ncbi.nlm.nih.gov/pmc/yabo214articles/PMC4365090/
为了证明固体制剂中Q1和Q2的等效性,处方方需要证明仿制药中含有与创新药相同浓度的相同成分。
分析通常使用定量技术,如高效液相色谱。
生物豁免的最后一个途径是Q3同一性,目前只适用于几乎没有系统性暴露风险的外用制剂,因此,分娩过程中的微小变化不太可能给患者带来风险。
拉曼成像
利用拉曼成像可以识别成分并定量,使其非常适合识别Q1和Q2的同一性。
虽然Q3的微观结构相同尚未适用于口服固体剂量,但Raman能够量化固体剂量形式的微观结构,包括颗粒/颗粒大小、均匀性和百分比覆盖率。也许使用拉曼成像来证明Q3的一致性可以成为一系列测试的一个方面,为将来口服固体剂量的生物豁免铺平道路?
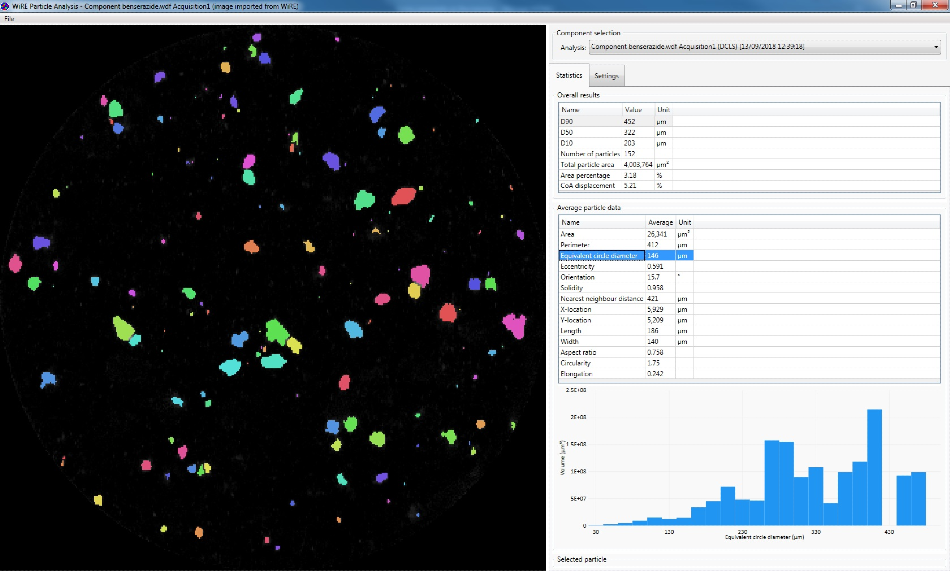
来自雷尼肖WiRE软件的粒子统计信息。
成千上万的拉曼光谱被收集到一个样品的表面,以确定一个配方的微观结构。一个采样点的所有化学信息都包含在每个像素中,它是由一个完整的拉曼光谱组成的。
任何表面,无论多么粗糙或光滑,都可以在保持图像聚焦的同时高速分析使用RA802制药分析仪结合雷尼肖的流线TM和LiveTrackTM技术。与传统拉曼系统相比,分析时间明显缩短,因为在全速时,系统可以每秒收集高达1500个光谱。
一旦收集了足够的光谱,就可以生成样品的完整化学图像,包括原料药、多态性、辅料、降解剂和污染物,并且可以使用假色分离所有必要的成分。
雷尼肖RA802药物分析仪。
比较创新者和通用产品
我们比较了两种平板电脑的拉曼图像,一种是创新平板电脑,另一种是普通平板电脑。
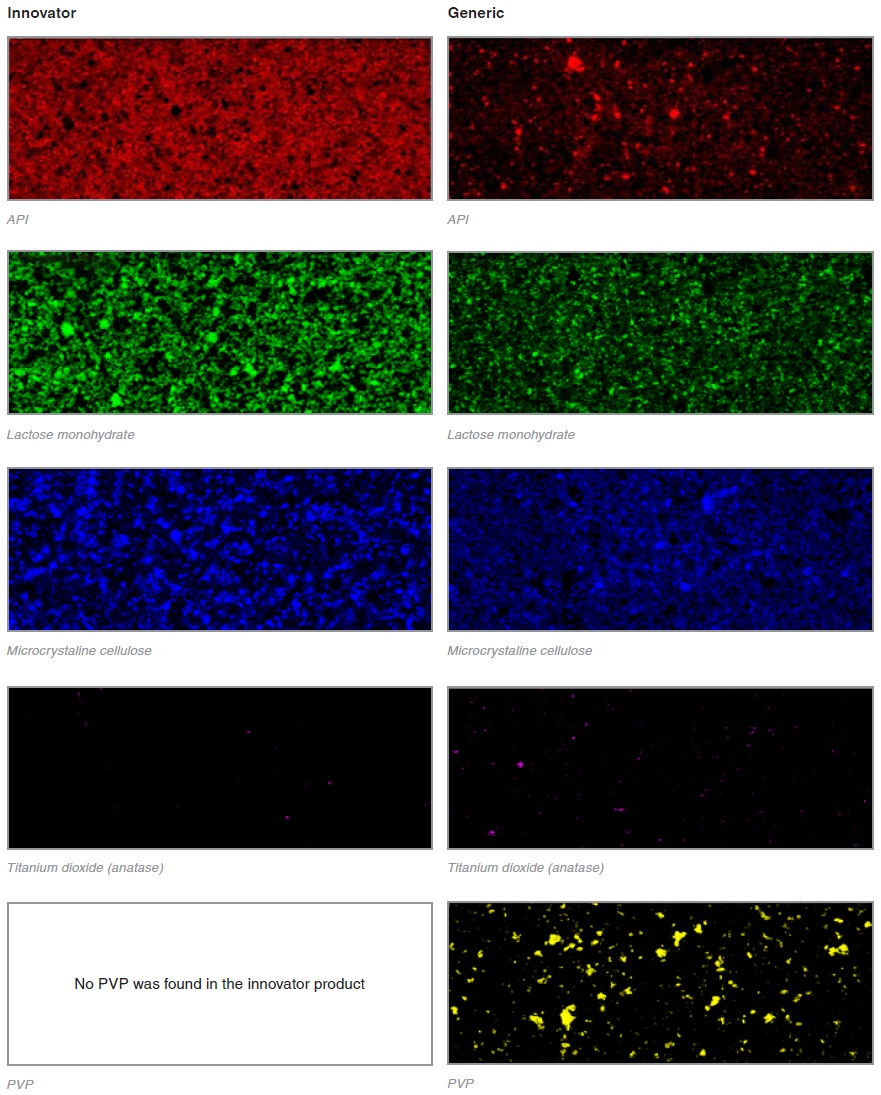
利用收集到的拉曼光谱对不同成分进行了鉴定。然后,为了便于比较,这些照片被涂上了假颜色,并分别展示出来。
一旦每个组件被识别,粒子统计分析可以在图像的域和粒子上执行。yabo214利用这些统计数据,可以对药片、批次和产品进行比较,以确定关键差异并诊断这些差异的原因。
颗粒大小
微晶纤维素(MCC)和乳糖的颗粒尺寸通过拉曼图像的数据进行比较,以确定是否有任何显著的差异。
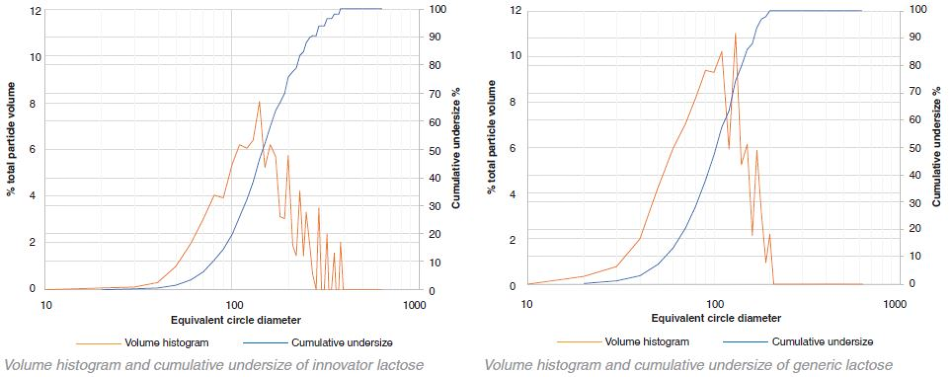
乳糖-创新者v一般体积直方图
乳糖-创新者v一般数字直方图
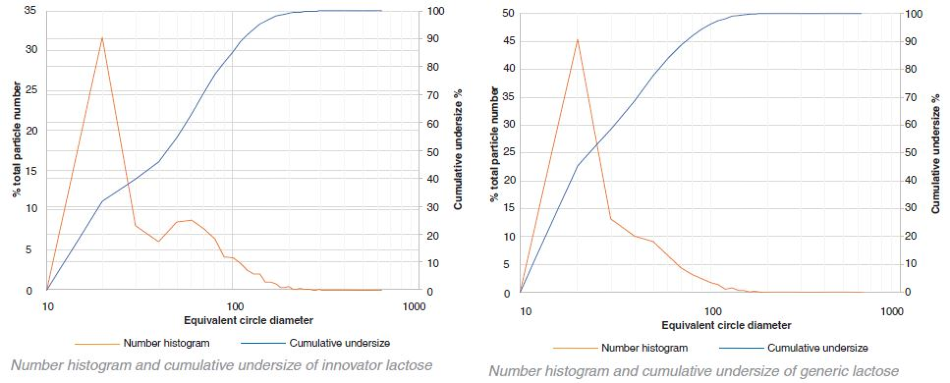
比较-创新者和普通乳糖-累积小
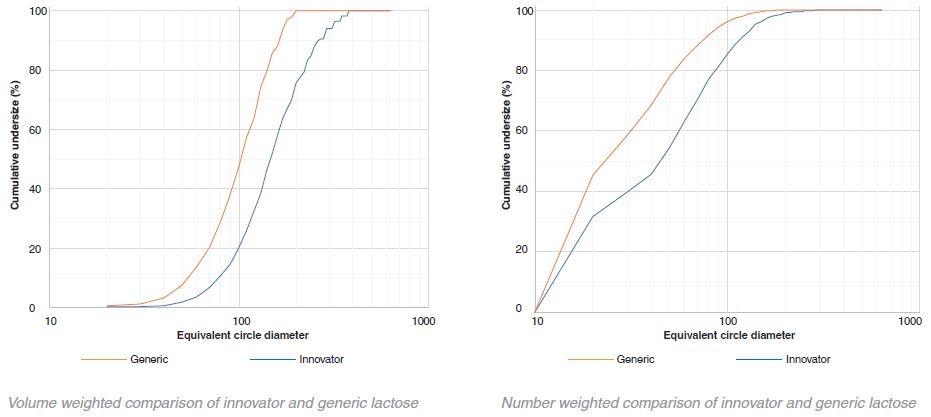
MCC -创新者v一般体积直方图
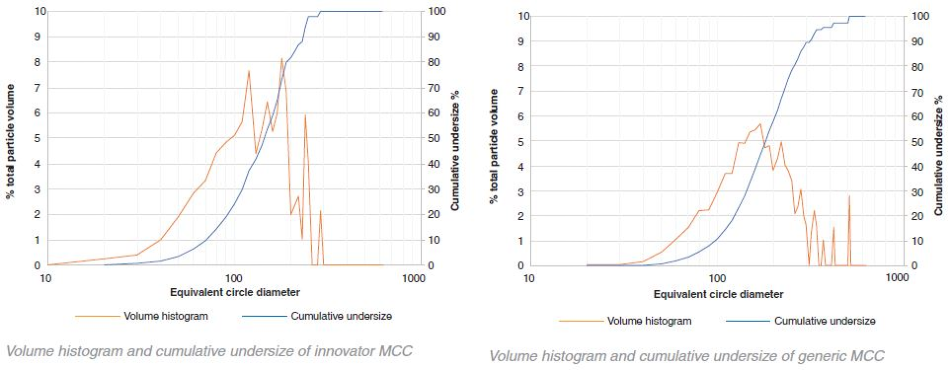
创新者v通用数字直方图
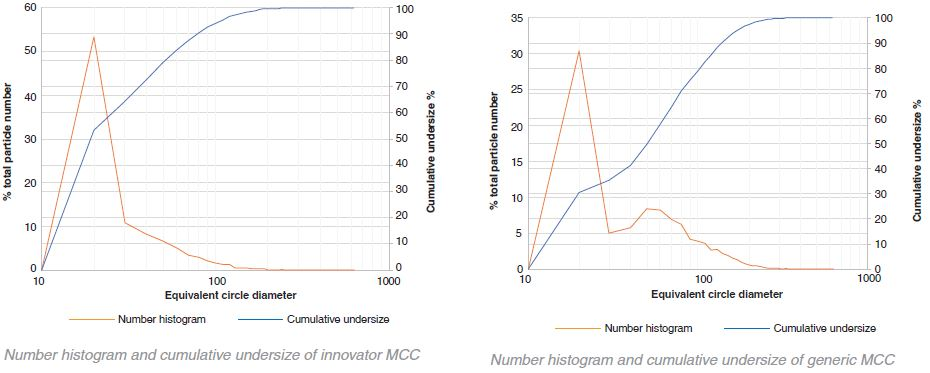
比较通用和创新者的MCC累积不足
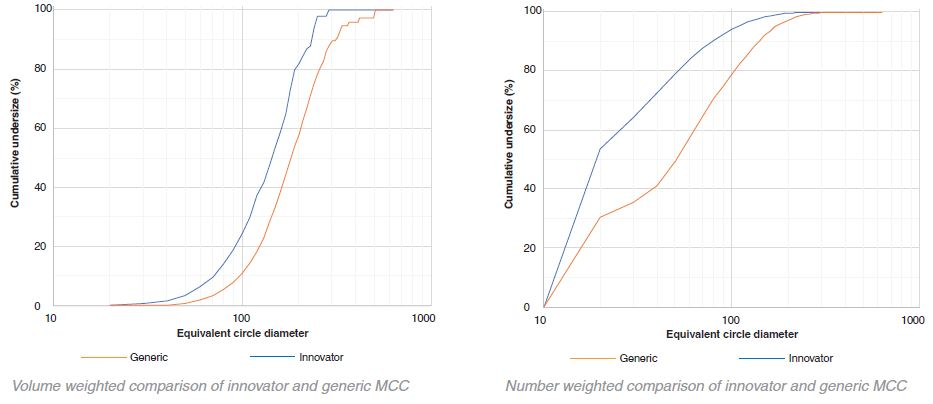
Generic与Innovator的比较
表2。
|
乳糖 |
世纪挑战集团 |
| 通用的 |
创新者 |
通用的 |
创新者 |
| D90 |
164µm |
253µm |
298µm |
218µm |
| D50 |
100µm |
142µm |
178µm |
135µm |
| D10 |
49µm |
76µm |
92µm |
63µm |
| 粒子数yabo214 |
7385 |
4702 |
4614 |
5936 |
| 我看 |
1.37% |
1.13% |
0.18% |
3.16% |
在乳糖的情况下,创新者的颗粒尺寸始终大于非专利产品。相比之下,MCC的仿制药颗粒尺寸大于创新药颗粒。然而,这种差异不像乳糖那样明显。体积直方图的变异性表明,在较高的颗粒尺寸时,一小部分非常大的团聚体占据了总体积的很大比例。
在仿制产品和创新产品中,MCC和乳糖颗粒都是高度多分散的,如图表数据所示。yabo214从数量上看,大多数的颗粒在10 μm - 20 yabo214μm之间(对于这个特定的样品收集,10 μm被设置为最小的颗粒尺寸分辨率)。然而,这些粒子yabo214只占总体积的一小部分。普通产品和创新产品中乳糖和MCC的体积加权D50值均在100 ~ 200 μm之间。
通过数字直方图显示了创新乳糖和通用MCC的一些双峰特性。大多数颗粒的尺寸为10 μm - 20 μyabo214m。然而,在50 μm - 60 μm之间,在两幅图中都出现了一个次级峰,表明颗粒在加入片剂混合物之前可能经过了筛分,以获得特定的粒径分布。yabo214
部件的均匀性由面积中心(CoA)表示。如果CoA为0%,那么在整个图像中,感兴趣的成分是均匀分布的,图像的中心是所有粒子的区域的中心。yabo214如果0%有任何偏移,则表示该成分分布不均匀。这也表明,更大比例的组件是偏重远离中心。
配方中普通乳糖和创新乳糖的辅酶a有很大的相似性。然而,就MCC而言,仿制药和创新药的CoA有显著差异。这些图像强调了为什么会出现这种情况。一般粒子具有更类似于网络的结构,相邻粒子之间的距离似乎比创新者之间的距离要小得多。yabo214
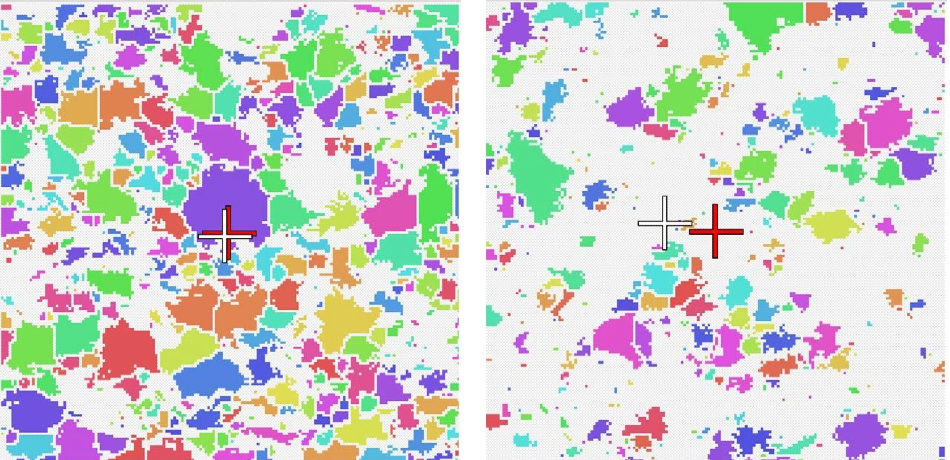
放大了从通用(左)和创新(右)MCC的区域中心(CoA)图像中提取的内容。红色的叉表示图像的中心,白色的叉表示CoA。在创新者的图像中可以看到更大的偏移。
讨论
表3。
| 创新者的成分 |
通用的成分 |
| API |
API |
| 乳糖一水 |
乳糖一水 |
| 二氧化钛(锐钛矿) |
二氧化钛(锐钛矿) |
|
聚乙烯吡咯烷酮(PVP) |
这两种产品的不同之处非常有趣。这些api的分发看起来甚至完全不同。拉曼成像的威力在这里得到了清晰的展示。即使没有关于这两种药片的背景知识,很明显这两种产品使用了非常不同的制造工艺。
这提出了一些问题,即混合和制片方法的差异可能导致这些差异。虽然API在创新产品中具有高度分散、模糊的结构,但API在通用产品中形成了谨慎、聚合的域。从视觉上看,通用产品是通常会看到的API分发类型的更典型的类型。
创新产品可能经历了湿造粒步骤,溶解或部分溶解了原料药,然后再结晶。这将导致更均匀的分散在整个配方。
拉曼成像的灵敏度可以通过含有小至1 μm的API颗粒和大团聚体的混合产品得到证实。yabo214用其他技术来实现这种识别是非常困难的。由于原料药不绑定在颗粒中,仿制片似乎使用简单的干粉末压实制备。
两种片剂均含有乳糖、微晶纤维素和二氧化钛。RA802有一个常见赋形剂的光谱数据库,使这些赋形剂易于识别。
另一个有趣的发现是,该非专利药片含有一种额外的成分:聚乙烯吡咯烷酮(PVP)。
这是不寻常的,因为仿制产品的目的是一个直接复制。它可能已经进入了一个创新者尚未推出的市场,或者计划将产品带向505(b)(2)路线。
PVP是一种结合剂,所以另一种解释是,通用变体的“粘性”较低,因此,配方师添加了额外的结合剂,试图提高平板电脑的稳健性。这些都只是推测。
虽然不太可能,但在某些特殊情况下,FDA可能会接受不同辅料的ANDA申报。然而,仿制药公司需要为其纳入提供一个合理的理由,并能够最终证明其与创新者在溶出度和生物等效性方面的药物等效性。
结论
创新者和一般产品可以成功地表征使用RA802.它也能够促进脱硝活动。
创新制剂的成分、浓度、颗粒大小和分布可以用RA802来表征,这允许仿制药追随者改变其工艺,以开发同等产品或战略上不同的产品。

该信息来源于,审查和改编的材料由雷尼肖plc -光谱学。亚博网站下载
欲了解更多信息,请访问雷尼肖plc -光谱学。